Para recordar las características de los sólidos, visita: http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/estados/solido.htm
No todos los sólidos son iguales ya que poseen propiedades específicas según su composición, estructura y enlace. Estas propiedades son:
- Elasticidad
- Dureza
- Fragilidad
- Estructura
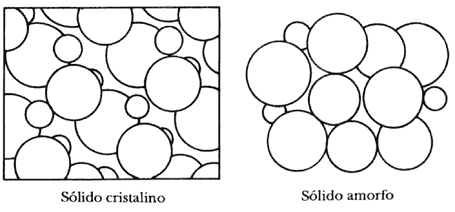
Estos materiales poseen una estructura desordenada, no tiene forma geométrica definida. También son llamados líquidos sobre-enfriados, ya que en realidad son líquidos altamente rígidos y viscosos, aunque posean propiedades físicas semejantes a las de los sólidos.


Estos materiales forman cristales que poseen una estructura
ordenada y repetitiva. Presentan
puntos de fusión fijos y propiedades físicas y químicas definidas.
puntos de fusión fijos y propiedades físicas y químicas definidas.

- Tipo de enlace
- Iónicos: Las partículas son iones presentes en la malla cristalina.Poseen una dureza característica que los hace quebradizos, se funden a altas temperaturas y son malos conductores eléctricos. Ejemplo: Cloruro de sodio.


- Moleculares:
Las partículas son moléculas que se entrelazan entre sí mediante fuerzas intermoleculares.
Presentan un punto de fusión bajo, son blancos y no son buenos conductores de la electricidad. Ejemplo: Metano

- Covalentes:
Red definida de átomos unidos entre sí mediante enlaces covalentes, siendo prácticamente imposible identificar una molécula individual en la estructura.
Presentan altos de fusión y no son conductores eléctricos. Ejemplo: Diamante.


- Metálicos:
Las partículas son iones positivos por electrones situados entre ellos. La nube electrónica que envuelve el total de iones, está formada por los electrones que no se encuentran unidos a ningún átomo sino que a todos en conjunto, los cuales se encuentran dispersos.
Presentan una buena conductividad eléctrica y térmica. Ejemplo: Hierro, Cobre



No hay comentarios:
Publicar un comentario